近日,濟南大學劉宏教授、王樹萍副教授聯合山東大學齊魯醫院周恒星教授及中國科學院深圳先進技術研究院王澤南研究員提出了一種納米藥物介導的“細胞內小分子/離子風暴”激活神經再生促進脊髓損傷修復的新方法。相關成果以“Intracellular small molecule/ion storm from Ca-phytate nanoparticle synergizes neural stem cell therapy and immunomodulation in spinal cord injury”為題發表在生物材料領域權威期刊Biomaterials(IF=12.9)。文章第一作者為濟南大學2022級碩士研究生時佳培、2024級博士研究生張朔和山東大學博士后馮彥斌,通訊作者為劉宏教授、王樹萍副教授、周恒星教授和王澤南研究員,濟南大學為第一完成單位。

脊髓損傷是一種毀滅性的中樞神經系統創傷,多由交通事故、高處墜落等意外事件引起。據統計,全球約有1500萬至2000萬人受其影響,每年新增病例近90萬。該疾病不僅導致患者感覺、運動和自主神經功能嚴重喪失,造成極高的致殘率,也為家庭和社會帶來沉重的經濟負擔。當前,脊髓損傷的治療面臨兩大核心挑戰:一是受損神經元固有的再生能力極弱,二是損傷區域持續的炎癥微環境嚴重阻礙修復進程。神經干細胞移植雖為再生帶來希望,但移植后的干細胞能否成功分化為功能神經元,以及如何應對“敵意”的炎癥環境,是決定療效的關鍵。因此,理想的治療策略需要“雙管齊下”:既能引導干細胞定向分化為神經元,又能將有害的促炎微環境逆轉為有益的修復型微環境。
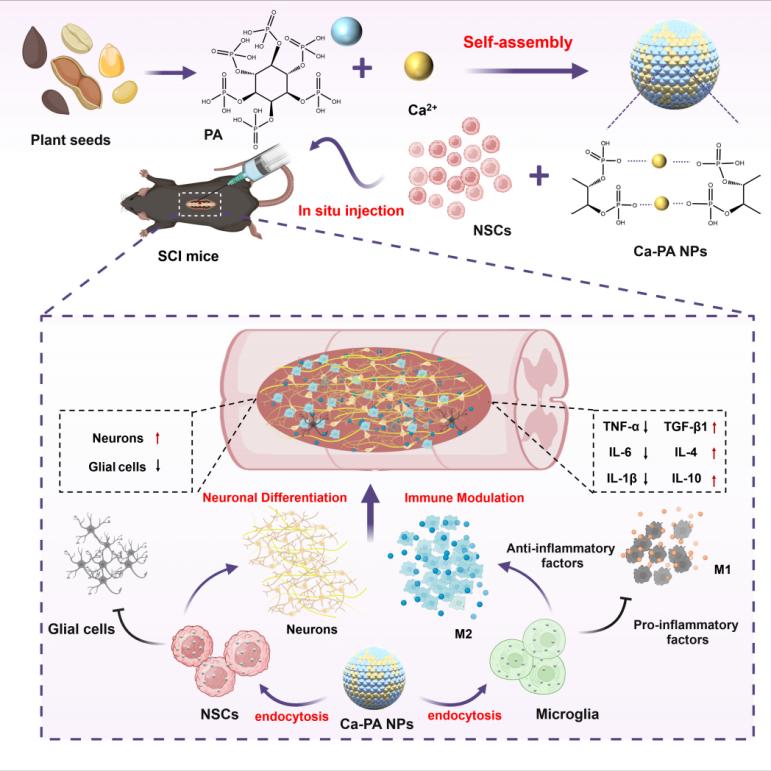
針對上述問題,研究團隊從天然產物中尋找靈感,設計了一種新型的智能響應型調節劑——植酸鈣納米藥物(Ca-PA NPs),其通過細胞內吞作用高效進入神經干細胞和小膠質細胞。在細胞內部的酸性溶酶體環境中,納米顆粒迅速分解,瞬間釋放出高濃度的游離植酸和鈣離子,形成“細胞內小分子/離子風暴”,實現對細胞命運的精準調控。該納米藥物不僅定向誘導神經干細胞向功能神經元分化,還可逆轉小膠質細胞從促炎M1表型向修復型M2表型重編程。在脊髓半橫斷損傷的小鼠模型中,納米藥物與神經干細胞共移植后,小鼠的后肢運動功能、感覺功能以及自主神經功能均得到顯著改善。損傷區域呈現功能性神經元再生及膠質瘢痕減少,同時炎癥細胞浸潤被有效抑制,神經再生微環境得到重塑。這項研究成功開發出一種新型納米調節劑,兼具精準調控干細胞命運與重塑免疫微環境的雙重功能,為開發用于脊髓損傷及其他神經系統疾病的下一代組合型納米藥物提供了全新思路與實驗基礎。通過功能化納米藥物的靶向性與遞送效率,該類創新制劑有望拓展至阿爾茨海默病、帕金森病等神經退行性疾病的治療領域,展現出重要的臨床轉化潛力。
近年來,劉宏教授帶領的濟南大學細胞診療與生物傳感器團隊在干細胞治療及生物檢測領域取得多項原創突破性研究成果(Adv.Mater.,Adv.Funct.Mater.,ACS Nano,Biomaterials,Adv.Sci.,Adv.Healthc.Mater.,Small,BMEMat)。相關工作得到了國家重點研發計劃、國家自然科學基金、國家高層次青年人才計劃、山東省自然科學基金、山東省泰山學者計劃、濟南市科技局和濟南大學的大力支持。
原文信息:
Shi J, Feng Y, Zhang S, et al. Intracellular small molecule/ion storm from Ca-phytate nanoparticle synergizes neural stem cell therapy and immunomodulation in spinal cord injury. Biomaterials. 2025. https://doi.org/10.1016/j.biomaterials.2025.123708
撰稿:王樹萍 編輯:劉孟頔 編審:張偉